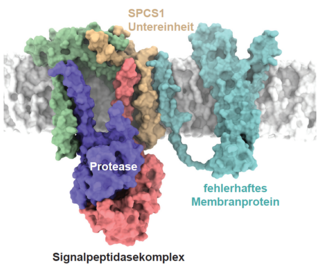
Forschende haben entdeckt, dass der Signalpeptidasekomplex, ein Enzym in unseren Zellen, die Qualitätskontrolle von Membranproteinen durchführt. Die Entdeckung dieser neuen Funktion eines Schlüsselenzyms in der Zellbiologie wurde in der Fachzeitschrift „Science“ veröffentlicht und könnte neue therapeutische Ansätze bei Alzheimer und anderen Krankheiten ermöglichen, bei denen Proteine fehlerhaft gefaltet werden.
Ein interdisziplinäres Team von Wissenschaftler*innen in Köln, Heidelberg und München hat eine neue Funktion eines altbekannten Enzyms entdeckt: Der Signalpeptidasekomplex im endoplasmatischen Retikulum spaltet fehlerhafte Membranproteine und leitet dadurch deren Abbau ein. Das endoplasmatische Retikulum in unseren Zellen ist für die Produktion und Kontrolle von Proteinen verantwortlich, die sezerniert, also von dieser Zelle freigesetzt werden. Der Signalpeptidasekomplex schneidet die Polypeptidketten, um die dafür nötigen Signalpeptide zu entfernen. Diese Signalpeptide ermöglichen es den Proteinen überhaupt erst, das endoplasmatische Retikulum zu erreichen, sodass die gereiften Proteine ihre spezifischen Funktionen erfüllen können. Ein Forschungsteam unter der Leitung von Matthias Feige, Professor für Zelluläre Proteinbiochemie an der Technischen Universität München, und Marius Lemberg, Professor für Biochemie an der Universität zu Köln, hat nun entdeckt, dass der Signalpeptidasekomplex für einen weiteren Schlüsselprozess der Zellbiologie verantwortlich ist: Er kontrolliert die Qualität von Membranproteinen. Das Forschungsergebnis ist unter dem Titel „The Human Signal Peptidase Complex Acts as a Quality Control Enzyme for Membrane Proteins“ in der Fachzeitschrift Science erschienen.
Jede Zelle ist von einer Lipiddoppelschicht umgeben, die das Innere der Zelle schützt. Eine Vielzahl von Zellfunktionen ist von einem geregelten Transport von Molekülen und Signalen durch diese Isolierschicht abhängig. Membranproteine sind in diese Lipiddoppelschicht integriert und erfüllen diese Funktionen. Sie sichern das Überleben der Zelle und dienen als wichtigste Ansatzpunkte für Medikamente. Um richtig zu funktionieren, müssen Membranproteine definierte dreidimensionale Strukturen mit atomarer Präzision korrekt ausbilden. Fehler in diesem Prozess können zu Krebs, Stoffwechselstörungen und neurodegenerativen Erkrankungen führen.
Das Team untersuchte mehrere krankheitsassoziierte Membranproteine unseres Nervensystems, um besser zu verstehen, wie unsere Zellen verhindern, dass fehlerhafte Proteine sie schädigen und Krankheiten verursachen. Im Forschungsverlauf stellten sie fest, dass eine Protease – ein Enzym, das andere Proteine spaltet – den Abbau von fehlerhaften, mutierten Proteinen einleitet. Dieser Abbau ist für die Aufrechterhaltung der zellulären Funktion unerlässlich. Sie konnten die verantwortliche Protease jedoch nicht identifizieren. „Alle bekannten Kandidaten und üblichen Hemmstoffe halfen uns bei der Suche nach dem zugrunde liegenden molekularen Mechanismus nicht weiter“, sagt Feige.
Der Durchbruch gelang, nachdem die Forscher*innen potenzielle Spaltstellen für den Signalpeptidasekomplex in den krankheitsverursachenden Proteinen identifizierten. „Die Lehrbücher besagen, dass der Signalpeptidasekomplex Signalpeptide während der Reifung von sekretorischen Proteinen abspaltet. Bisher galt das als seine einzige Funktion“, fügt Lemberg hinzu. Nun erwies sich der Signalpeptidasekomplex jedoch als die gesuchte Protease, die für die Qualitätskontrolle von Membranproteinen verantwortlich ist.
Basierend auf dieser Erkenntnis identifizierte das interdisziplinäre Team weitere Proteine, die gespalten werden, und zeigte, dass ein bestimmter Bestandteil des Signalpeptidasekomplexes, die SPCS1-Untereinheit, diesen Vorgang reguliert. „Da diese Untereinheit für seine ursprünglich beschriebene Rolle bei der Proteinreifung nicht notwendig ist, wurde uns klar, dass wir es mit einer bisher unerkannten Funktion zu tun haben“, erklärt Feige.
SPCS1 gehört zu den drei Genen, die in allen Gehirnregionen bei der Alzheimer-Krankheit herunterreguliert sind. „Das deutet darauf hin, dass unsere Ergebnisse wichtige Auswirkungen auf unser Verständnis der menschlichen Biologie und altersbedingter Erkrankungen haben könnten“, fügt Lemberg hinzu. Bei Alzheimer sammeln sich fehlerhafte Proteine an, die vermutlich die neuronale Funktion beeinträchtigen. Feige schließt: „Unsere Ergebnisse helfen besser zu verstehen, wie Zellen die molekulare Struktur ihrer Proteine kontrollieren, und bilden die Grundlage für viele künftige Studien.“
Die Forschung wurde vom Bundesministerium für Bildung und Forschung (BMBF), der Deutschen Forschungsgemeinschaft (DFG) und der Fritz Thyssen Stiftung gefördert.
Inhaltliche Kontakte:
Professor Dr. Marius Lemberg
Zentrum für Biochemie und Exzellenzcluster für Alternsforschung CECAD, Universität zu Köln
+49 221 478 77288
m.lemberguni-koeln.de
Professor Dr. Matthias Feige
Center for Functional Protein Assemblies (CPA), Department of Bioscience, TUM School of Natural Sciences, Technische Universität München
+49 89 28913667
matthias.feigetum.de
Presse und Kommunikation:
Eva Schissler
+49 221 470 4030
e.schisslerverw.uni-koeln.de
Link zur Studie:
https://www.science.org/doi/10.1126/science.abo5672
Pressemitteilung der Universität zu Köln